\欲しい魚も用品もcharmでだいたい見つかる!/
〜ネコポス対応で単品購入の送料が安い商品多数!〜
今回の内容を動画にまとめました。
よろしければご覧ください。
今回はろ過の話です。
アクアリウムをやるなら「ろ過」の知識はあったほうがいいでしょう。
ろ過には「物理ろ過」「生物ろ過」「化学ろ過」
があります。
今回はろ過の中で最も重要な
「生物ろ過」
に着目して、その仕組みを解説していきます。
アンモニアについての内容が多めです。
ちなみに物理ろ過というのはゴミなどをフィルターでこし取るろ過。
化学ろ過はゼオライトなどに有害物質などを吸着させるろ過です。
今回は物理と化学のろ過は割愛します。
生物の遺体や排泄物は分解されてアンモニウムイオン
NH4+
を発生させます。
これがかなり毒性のある物質です。
そしてそれが分解されて亜硝酸イオン
NO2–
になります。これはアンモニウムイオンよりは毒性は低いですが、それなりに毒性があります。
そしてこれがさらに分解されて硝酸イオン
NO3–
になります。
硝酸イオンまでアンモニウムイオンが分解されると、とりあえず生物は生活できます。
ただしこれも亜硝酸イオンより毒性は低いですが、過剰になると毒性があります。
アクアリウムでは普通、硝酸イオンが分解されるということはないので溜まる一方です。
水草が多少利用しますが、発生するすべての硝酸イオンを消費するほどではありません。
アクアリウムでは水換えで硝酸イオンを水槽の外に排出されることで、魚の健康を守っています。
溜まるたびに薄めているんです。
ここまでの
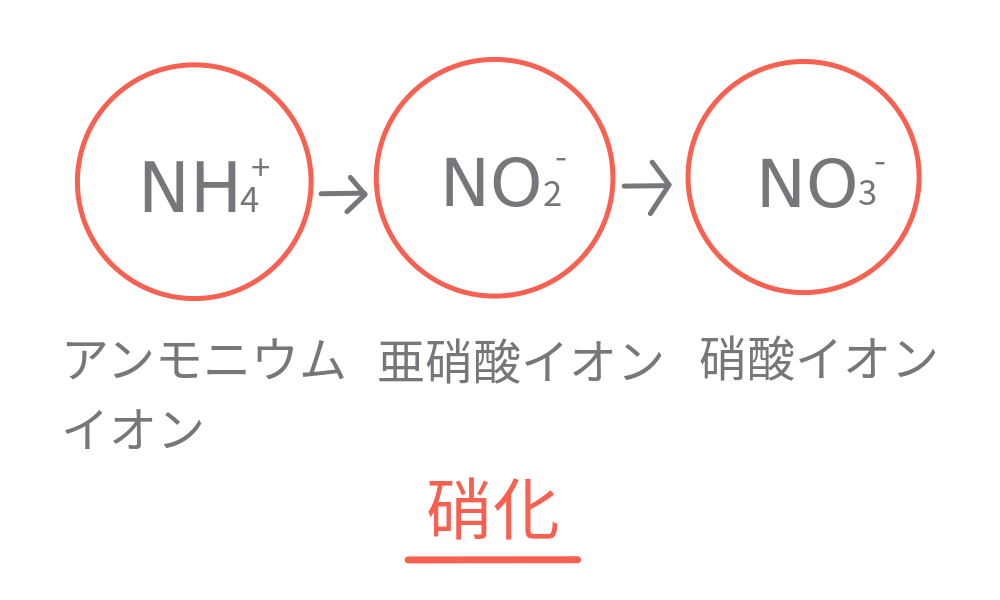
アンモニウムイオン→亜硝酸イオン→硝酸イオン
の変化は
「硝化」
と呼ばれています。

この硝化を行うのが生物ろ過です。
生物ろ過ができないと魚は生活できません。
なので重要なろ過なのです。
水槽を買ってきて、水槽に水を入れて、フィルターを回せば、その日からこの硝化ができるというわけではありません。
硝化にはアンモニウムイオンを亜硝酸イオンに分解する
「亜硝酸菌」
と亜硝酸イオンを硝酸イオンに分解する
「硝酸菌」
という二つの菌が必要です。
この二種類の菌は自然界のそこらじゅうにいるので、買ってくる必要はないんですけど、餌を与えて増やさないといけないんです。
水槽に水を入れただけだと、二種類の菌はほぼゼロです。
なのでまず
この段階を踏まなければいけません。
亜硝酸菌と硝酸菌を増やして、飽和させれば水槽は「完成」します。
完成すれば魚に餌を与えてアンモニウムイオンが発生してもすぐに分解される良い水になります。
完成させるまでの期間ですが、早くて2週間、遅くて一ヶ月くらいです(1)。
(1)参考:エーハイム, エーハイムで魚に危険なアンモニア亜硝酸を解消, 閲覧日:2023-01-21.
アクアリウム初心者によく起こる失敗は、水を完成させずに水槽をセットして、餌を食べる姿が楽しくてセット初日から餌を大量に与えることです。
硝化ができていないので、アンモニウムイオンが増加する一方となり、生体にダメージが生じて弱って病気になったりします。
気をつけましょう。
ちょっとアクアリウムに詳しい人は
「パイロットフィッシュ」
という丈夫な熱帯魚を水槽立ち上げ時に導入するというのを聞いたことがあるかもしれません。
パイロットフィッシュにはアカヒレが選ばれることが多いですね。
丈夫なので、多少過酷な環境でも生きられます。
水槽をセットしたら、本当に入れたい熱帯魚は買わずに、まずパイロットフィッシュを入れて餌を少なめに与えて、亜硝酸菌と硝酸菌を増やして水槽を完成させ、その後に本当に入れたい魚を買ってきて導入する。
こういうことをやります。
この二種類の菌は水の中でも増えますけど、多くは「フィルターのろ材」「底床の砂利やソイルの中」で増えて定着します。
フィルターを買うとろ材が付いてきます。

投げ込み式フィルターのフワフワした部分とか、スポンジフィルターのスポンジ、外部式フィルターの多孔質のリングやボール状の石みたいなやつ。
こういうろ材は表面積が大きいです。
中に微細な穴が空いているので、それだけ表面積が多くなります。
形によって表面積が増えるという話は以前このブログでも取り扱いました。
よろしければそちらもご覧ください。
>微生物の力?なぜ油膜にエアレーションが有効なのか考えてみた
表面積が大きくなれば、それだけたくさんの菌が付着できるので、ろ過力が高くなります。
だからフィルターにはろ材が必要なのです。
ゴミをこし取るだけなら、薄いウールを筒に詰めて、そこに水を流すだけで完成です。
しかし生物ろ過のための菌をたくさん増やすために、ある程度の量のろ材が必要なのです。
また砂利も同様の理由でただの平面よりは表面積が稼げるので意外に表面積があります。
ソイルはそれに加えて、ソイル内に微細な空間がたくさんあるので、さらに表面積があります。
底床もこの理由で必要な場合が多いです。
ベアタンクが難しいのはこの辺にも原因があります。
高校の生物(Ⅱの範囲だと思います)で習うんですけど、亜硝酸菌と硝酸菌は
「化学合成細菌」
と呼ばれていて、酸素を使ってアンモニウムイオンや亜硝酸イオンを酸化させて活動エネルギーを獲得します。
亜硝酸菌の反応は
2NH4++3O2→2NO2–+4H++2H2O+化学エネルギー
硝酸菌の反応は
2NO2–+O2→2NO3–+化学エネルギー
このように酸素を使ってエネルギーが発生します。
なので水槽にはある程度の酸素が必要です。
でないと二種類の菌が活動できなくなって、生物ろ過が弱くなります。
よく水草水槽では夜間エアレーションをするといいと言われます。
これは水草水槽の次の特性によるものです。
つまり夜間は酸素が足りなくなるので、生体が酸欠になるというものです。
酸欠になるのは亜硝酸菌と硝酸菌も一緒なので、夜間にろ過力が低下します。
だからろ過力を維持して、夜間にも生体から発生するアンモニウムイオンを分解させるために夜間の酸素供給用のエアレーションをすべきという話になります。
ちなみに普通は夜間は光合成しないのでCO2の添加はOFFにします。
水草水槽でないなら、エアレーションは一日中やっておいたほうがいいでしょう。
エアレーション関係で油膜について書きました。
よろしければそちらもご覧ください。
>微生物の力?なぜ油膜にエアレーションが有効なのか考えてみた
ここからは高校の化学(Ⅱの範囲)の話が入ってきます。
アンモニウムイオンは水中では
「アンモニア:NH3」
と
「アンモニウムイオン:NH4+」
の二つの状態で存在しています。
NH3+H2O⇄NH4++OH–
水中ではこの左辺と右辺の状態で
「電離平衡」
の状態にあります。
左辺と右辺の量的な割合はあるpHに対して一定となっていて、左辺が増えると左辺が減少する方向、つまり右辺が増える方向に反応が進むという関係があります。
これを
「平衡移動」
と呼びます。
例えば餌が分解されて右辺のアンモニウムイオンが増えたら、アンモニウムイオンが減少して、左辺のアンモニアが増えるような状態になります。
アンモニアのほうがアンモニウムイオンより毒性が強いので、アンモニウムイオンの増加は望ましくありません。
また電離平衡状態の左辺と右辺の割合はpHによって変わります。
pHが低いほうがアンモニウムイオンの割合が大きくなり、pHが高くなるにつれアンモニアの割合が増えます。
淡水魚水槽ではpHはだいたい中性の7です。
この状態ならアンモニウムイオンがほとんどなので、アンモニアの心配はあまりいらないです。
しかし海水魚水槽ではpHが8くらいになるのでアンモニアの割合が増えます。
淡水魚水槽の感覚でろ過を考えていると、同じ量の餌を与えてもアンモニアの害が大きくなるので注意が必要です。
また大磯砂などには貝殻が入っているため、これが溶けるとpHが上がります。
立ち上げ初期に新品の大磯砂を使うとpHが上がって、アンモニアの割合も増えるので気をつけましょう。
では実際にどのくらいの割合になるのかという計算をしてみます。
次の文献(2)によるとpHによるアンモニアの割合(%)は次の式で計算できます。
(2)参考:山 形 陽 一 ・ 丹 羽 誠,日本ウナギに対するアンモニアの急性および慢性毒性, Bulletin of the Japanese Society of Scientific Fisheries 48(2), 171-176, 1982.
NH3の割合(%)=100÷(1+10pKa-pH)
ここで25℃のときのpKa=9.25を使います。
ちなみにアンモニウムイオンの割合は
100-NH3の割合(%)
で計算しました。
この式でpH=7を計算すると
NH3の割合(%)=0.56%
pH=8で計算すると
NH3の割合(%)=5.3%
つまりpH=7のときは
NH3:0.56%
NH4+:99.44%
pH=8のとき
NH3:5.3%
NH4+:94.7%
海水魚水槽は淡水魚水槽の約10倍NH3が発生すると考えられます。
※追記
じゃあ実際にpH7のときのアンモニア0.56%というのは安全かというのが気になりますよね。
一般に淡水魚の全アンモニアの限界量は0.2mg/Lとされています。
それによりますと、全アンモニアは環境基準と要監視項目に該当しない有害物質の基準値として、淡水域では0.2mg/l、海水域では0.3mg/lとされています。
一般財団法人環境イノベーション情報機構, アンモニアの水産用水基準について
これは全アンモニア(アンモニアとアンモニウムイオンの総量)ですけど、以下の文献ではアンモニアの限界値を0.02[mg/L]としているので、アンモニアが0.02[mg/L]で危険と考えて良いでしょう。
水生生物に対する急性毒性試験や慢性毒性試験の結果より,水生生物が正常に生息し繁殖するためには,NH3濃度として少なくとも0.02NH3 mg/l 以下を維持することが必要であると判断し,この数値をリスク評価指針値とした。
菊地幹夫, 若林明子, アンモニア汚染の環境リスク評価, 東京都環境科学研究所年報 1997年
これを当てはめてみると、アンモニアとアンモニウムイオンの合計量x[mg/L]があったときにその0.56%が0.2[mg/L]になる値を求めてみると
x×0.0056=0.02より
x=0.02/0.0056≒3.57[mg/L]
ここで給餌量によってどのくらいTAN(Total Ammonia Nitrogen:アンモニアとアンモニウムイオンの合計)が発生するかですが、以下の文献によって計算式が公開されています。
PTAN=F*PC*0.092 (1)
where:
James M. Ebeling a, Michael B. Timmons b,J.J. Bisogni c, Engineering analysis of the stoichiometry of photoautotrophic, autotrophic, and heterotrophic removal of ammonia–nitrogen in aquaculture systems, Aquaculture Volume 257, Issues 1–4, 30 June 2006, Pages 346-358
PTAN
Production rate of total ammonia nitrogen, (kg/day)
F
Feed rate (kg/day)
PC
Protein concentration in feed (decimal value)
ここでPCは餌のタンパク質含有率ですが、普通は45%程度です。以下のキョーリンのネオプロスは48%程度のようです。つまりPCは0.45程度でいいでしょう。
ここで例えば45cm規格水槽の水量を30Lとします。水槽水量の表は以下の記事をご覧ください。

3.57*10-3[g/L]=F*103[g/day]*PC*0.092/(30[L])
ゆえにF≒0.00259[kg/day]
一日に45cm規格水槽に2.6g餌を放り込むと危険な水準になる計算です。
一般にアンモニウムイオンが検出されなくなるまでの硝化サイクルにおける日数は約14日です。(参考:「チョコ断ち実験室」。, 生物濾過サイクルが出来上がるまでのアンモニアと亜硝酸の推移。)
つまり2.6gを14で割った数値が一日に投入可能な餌のマックスになります。
2.6÷14≒0.186[g]
一日0.186[g]を45cm規格水槽に投入するとマズそうです。
通常の金魚の飼育では1.5%~2%の給餌を推奨しているので、3%は相当大量の給餌量と言えます。
キョーリン, 給餌方法でらんちゅうの成長と体形はどう変わるか
例えば45cm規格水槽の場合、金魚の適正匹数は以下の記事からだいたい6匹とします。

5cmの金魚の体重は約3[g]です。(参考:金魚のマルウ, サイズ&グラム表)
6匹の合計体重は18[g]程度ですから、この2%を給餌量とすると、0.36[g]が一日の給餌量となります。
一日0.186[g]を45cm規格水槽に投入するとマズそうと言ったので、正直微妙ですね。
確かにアンモニウムイオンは徐々に増えて、徐々に減るので単純に掛け算で増えるわけではないのですが、単純に餌から発生するアンモニアとアンモニウムイオンの量を考える場合、ちょっと危ないような気がします。
魚の数が45cm規格水槽で3匹とか半分になれば帳尻が合いますけど、やっぱりある程度水換え頻度を上げるとかしておいたほうがリスクは減るような気がしますね。
以下立ち上げ初期の水換え頻度などの記事です。そちらも参考にしてみてください。

また実際の水槽の全アンモニアの測定値を計測したサイトとして以下を考えます。
参考:かわいいクロサンショウウオ, 1999. 8.10 順調なファーストステップ
このサイトによると立ち上げ初期の全アンモニアの量は最高で1.5mg/L程度になります。
この値は前述の0.2mg/Lを超えるのであんまりよくないですね。
確かにアンモニアがこの0.56%とすると0.0084mg/L程度になり、0.02mg/Lよりかなり少ないんですけど、完全に安心できる状態ではないような気がしますね。
※追記終わり
上の計算で、アンモニアの割合はpH=7だと8のときの10分の1になるので、pH=7だとアンモニアは心配いらないという話がたまにあるんですけど、アンモニウムイオンが大量にあれば上の平衡移動の原理からアンモニアの量も増えるのでpHの影響が薄まっていきます。
アンモニウムイオンを大量に溜めるというのはよくないですね。
生物ろ過をしっかりやりましょう。
またアンモニウムイオンに毒性はほぼないという話は割と有名なのですが、アンモニウムイオンそのものにも毒性の寄与はあるという研究もある(3)ので、油断しないほうがいいでしょう。
ミジンコの話ですけど、水生生物ですからね。
(3)参考:(学) 根本佳介 1)、幡野亜由美 1)、(正) 庄司良 1)、(正) 山田正人 2)、(正) 成岡朋弘 2)
1) 東京工業高等専門学校、2) 国立環境研究所, 廃棄物処分場浸出水におけるアンモニアの形態変化を考慮した毒性の解析, 第20回廃棄物資源循環学会研究発表会セッションID: D5-1, 2009.
今回は生物ろ過についてその仕組みとそれを担う菌の解説や関連物質の計算などを行いました。
生物ろ過に関して知識が深まれば幸いです。
生物ろ過をしっかり行って、生体が住みやすい環境を作りましょう。